SIBO (&co) et MAI, liens et pistes de réflexion
- Juliette Janvresse

- 15 avr.
- 11 min de lecture

Le SIBO est de plus en plus exploré comme facteur potentiel dans la physiopathologie de certaines maladies auto-immunes. Cet article a pour but de présenter ce qu’est le SIBO, ses symptômes, sa mise en évidence clinique et ses liens avec les maladies auto-immunes (MAI).
Zoom SIBO, IMO, LIBO, SIFO... comment s’y retrouver
Derrière ces acronymes se cachent différentes formes de dysbioses, c’est-à-dire des déséquilibres du microbiote intestinal selon la localisation et le type de micro-organismes impliqués.
SIBO (Small Intestinal Bacterial Overgrowth) : prolifération excessive de bactéries dans l’intestin grêle. On distingue principalement le SIBO à hydrogène (H2) et le SIBO à hydrogène sulfuré (H2S), ce dernier étant plus rare.
IMO (Intestinal Methanogen Overgrowth) : prolifération d’archées méthanogènes (micro- organismes distincts des bactéries) productrices de méthane, pouvant affecter l’ensemble du tube digestif.
LIBO (Large Intestinal Bacterial Overgrowth) : excès de bactéries dans le côlon.SIFO (Small Intestinal Fungal Overgrowth) : prolifération excessive de levures ou de champignons
dans l’intestin grêle.
Dans cet article, nous nous focaliserons principalement sur le SIBO à hydrogène, le plus étudié dans le contexte des maladies auto-immunes.
Manifestations cliniques du SIBO H2
Le SIBO n’est pas causé par des bactéries pathogènes, mais par une prolifération excessive de bactéries. Ces bactéries fermentent de manière rapide et excessive les glucides fermentescibles (notamment les FODMAPs), entraînants divers symptômes digestifs.
Les manifestations les plus fréquentes incluent (Bures et al., 2010(Frasier et al., 2025)) :
douleurs abdominales
flatulences excessives
ballonnements et distension abdominale (“ventre de femme enceinte »), qui se manifestent
rapidement après le repas
reflux
constipation et/ou diarrhée (plus souvent des diarrhées dans le cadre de SIBO*)
alternance diarrhée-constipation
nausées
Rosacée, dermatite atopique
Certains éléments cliniques orientent vers cette hypothèse :
apparition des symptômes quelques mois après une gastro-entérite
suite à la prise d’inhibiteurs de la pompe à protons, d’opioïdes ou d’antibiotiques
après une chirurgie abdominale
amélioration transitoire sous antibiotiques
aggravation après la prise de probiotiques chez certains patiente
aggravation de la constipation par les fibres fermentescibles
Les causes
Le corps a plusieurs systèmes de défense permettant d’éviter la prolifération de bactéries dans le grêle (Pimentel et al., 2020). Parmi elles ont retrouvent :
L‘acide chlorhydrique (acide de l’estomac) dont les rôles sont de tuer les microbes ingérés lors de la consommation d’aliments, d’activer les enzymes digestifs et de déclencher la libération d’enzymes et de bile par le pancréas et la vésicule biliaire
La bile, indispensable à l’absorption des graisses, qui joue également un rôle antimicrobien
Les enzymes protéolytiques qui vont découper les aliments et détruire les bactéries dans
l’intestin grêle
Des défenses mécaniques : valve iléocaecale entre l’iléon (dernière partie de l’intestin grêle) et le caecum (première partie du gros intestin) qui empêche les bactéries de « remonter » (bien que cette hypothèse semble moins probable)
Le complexe migrant moteur, véritable balai digestif qui par ses contractions « poussent » les bactéries et les résidus alimentaires vers la « sortie »
Le mucus intestinal qui joue un rôle de barrière et est crucial dans l’équilibre du microbiote
Le système immunitaire et notamment les IgA sécrétoires
Si l’un des systèmes devient défaillant, même de façon temporaire, le risque de développer un SIBO augmente.
Pourquoi ces systèmes de defenses échouent ?
Certains médicaments et facteurs issus d’anomalies favorisent l’apparition du SIBO. Le SIBO est un trouble souvent associé d’autres, telles que (Bures et al., 2010; Pimentel et al., 2020) :
Anomalies anatomiques :
Maladie de Crohn, maladie cœliaque non diagnostiquée ou pas contrôlée ;
Diverticules
Chirurgies, telles qu’une restriction des intestins ou du côlon (ex : bypass)
Endométriose
Anomalies fonctionnelles :
Prise chronique d’inhibiteur à protons (médicament prescrit en cas de reflux, brûlures d’estomac)
Faible acidité gastrique
Mouvement intestinaux lents, pouvant être dus à la prise de certains médicaments,
au stress, à une réaction type auto-immune ou à du grignotage intempestif
perturbant le complexe moteur migrant
Dysfonctionnement de la valvule iléo-caecale (« petite porte » entre l’intestingrêle et le côlon).
Autres :
Suite d’une radiothérapie pelvienne ou abdominale
Production insuffisante d’enzymes digestives par le pancréas (IPE)
Expositions fréquentes aux antibiotiques
Prise de contraceptifs hormonaux
Déficience immunitaire
Troubles thyroïdiens
Post infectieux. C’est l’une des causes les plus fréquentes en cas de SIBO, mais qui
apparait notamment sur microbiote peu résilient.
Le SIBO est un symptôme souvent multifactoriel et lié à une autre condition. Il apparait quand un, ou plusieurs systèmes de défenses de l’organisme sont rompus.
Mise en évidence biologique du SIBO
Le Graal en matière de diagnostic est le prélèvement de fluide de l’intestin grêle et de compter les bactéries présente. Cette méthode est peu commune, car elle est extrêmement invasive et coûteuse.
De plus le résultat du test peut être faussement négatif, car l’échantillon ne reflète pas ce qui se passe au niveau de l’extrémité distale de l’intestin grêle (vers le gros intestin), car l’échantillon est prélevé au niveau du duodénum (partie haute de l’intestin grêle).
Aussi, en pratique on utilise un test respiratoire. Le but de ce test est d’ingérer un sucre (glucose ou lactulose) et d’expirer dans un petit sac toutes les 20 minutes pendant 3h (pour le lactulose). Cela permet de suivre le trajet du sucre dans le tube digestif.
On va mesurer 2 gaz : l’hydrogène et le méthane (+CO2, mais ce dernier permet uniquement de vérifier la fiabilité du test).
Selon les taux expirés ont pourra conclure à un SIBO et/ou IMO (il est possible d’avoir les 2). La lecture de ce test doit être « bien » réalisée.
Selon les taux, on pourra suspecter un SIBO H2S. Cette hypothèse pourra être vérifiée via l’analyse métagénomique du microbiote et toujours corréler à la clinique (symptômes).

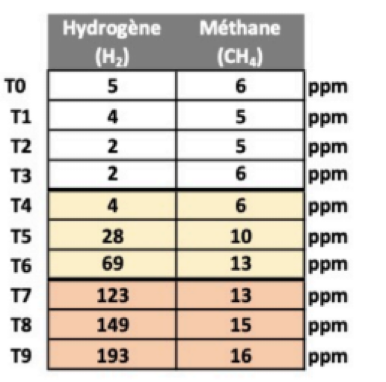
Résultats d’un test SIBO/IMO au lactulose
Traitement
Le traitement proposé en médecine « classique » est l’antibiothérapie (Pimentel et al., 2020). Toutefois, chercher uniquement à éliminer l’excès de bactéries sans comprendre la/les causes et agir sur celle(s)/ci est un risque d’échec.
Selon les études, 30% à 40% des patients n’auraient pas de résolution des symptômes de SIBO sous antibiotiques et les récidives toucheraient 45% des personnes ayant eu recours à l’antibiothérapie (les personnes âgées, celles sous IPP et post ablation de l’appendice sont plus à risques (Lauritano et al., 2008).
La prise en charge du SIBO s’articule autour de plusieurs axes et notamment :
soutien de la digestion et de la motilité intestinale
réduction de la pullulation microbienne
réparation de la muqueuse intestinale
correction des carences nutritionnelles
prise en compte des facteurs hormonaux et immunitaires
stratégies nutritionnelles adaptées (et notamment correction des carences très fréquentes en cas de SIBO).
Pour cela, nous disposons de nombreux outils en médecine fonctionnelle. On utilisera l’alimentation, la micronutrition, la phytothérapie et les thérapies manuelles principalement.
SIBO & maladies auto-immunes
Les personnes atteintes de maladie auto-immunes sont plus à risque de développer un SIBO. Une méta-analyses conduite sur 720 personnes atteintes de MAI a montré qu’au total, 75 % des patients présentaient un test respiratoire positif. Parmi eux, le taux de positivité était de 69% chez les patients atteints de polyarthrite rhumatoïde, 69% chez ceux atteints de lupus érythémateux systémique, 79% pour le syndrome de Sjögren, 89% pour la spondylarthrite ankylosante et 73% pour l’arthrite juvénile idiopathique (Shang et al., 2019).
Pourquoi ces chiffres ?
D’abord, beaucoup de MAI s’accompagne de troubles de la motricité digestive. Certaines MAI (sclérodermie, diabète auto-immun, hypothyroïdie auto-immune, etc.), l’inflammation, la neuropathie autonome ou les atteintes musculaires lisses ralentissent ce mouvement.
Ensuite, il y a la question immunitaire locale. L’intestin grêle dépend fortement de l’immunité muqueuse (IgA sécrétoires, peptides antimicrobiens, intégrité de la barrière). Dans les MAI, cette immunité est souvent dérégulée. On observe un système immunitaire hyper réactif et s’attaquant au « soi ». En parallèle, le système immunitaire peut être plus permissif face à certains microbes. Résultat, les bactéries opportunistes colonisent des zones où elles ne devraient pas être en grand nombre.
Troisième facteur : les médicaments. Corticoïdes, immunosuppresseurs, anti-TNF, IPP... modifient l’écosystème digestif.
Il faut aussi considérer les altérations anatomiques et fonctionnelles associées : chirurgies digestives, adhérences, diverticules, ralentissement du transit, insuffisance pancréatique exocrine, cholestase... Toutes ces situations sont plus fréquentes dans certaines MAI et favorisent la prolifération bactérienne.
Enfin, il existe probablement un cercle vicieux bidirectionnel. Le SIBO augmente la perméabilité intestinale et l’exposition aux endotoxines bactériennes (LPS), ce qui peut stimuler ou aggraver l’auto-immunité chez des personnes génétiquement susceptibles.
Le SIBO peut, dans certains cas, résulter d’un mécanisme auto-immun déclenché par une intoxication alimentaire (Xiao et al., 2021). Des bactéries entéropathogènes telles que Escherichia coli, Campylobacter jejuni ou Salmonella produisent notamment une toxine appelée cytolethal distending toxin B (CDT-B).
Lors d’une gastro-entérite aiguë, le système immunitaire fabrique des anticorps dirigés contre ces bactéries et leurs toxines afin d’éliminer l’infection. Habituellement, ces anticorps diminuent une fois l’agent pathogène éradiqué. Cependant, chez certaines personnes, une réaction croisée peut survenir : les anticorps anti-CDT-B reconnaissent également la vinculine, une protéine impliquée dans la fonction neuromusculaire du complexe moteur migrant (CMM), essentiel à la clairance bactérienne de l’intestin grêle.
Cette atteinte perturbe la motilité intestinale et favorise la stagnation du contenu de l’intestin grêle, créant un environnement propice à la prolifération bactérienne.
Ce mécanisme post-infectieux pourrait expliquer l’apparition d’un SIBO plusieurs mois après un épisode de gastro-entérite aiguë.
Sur le plan physiopathologique, la situation peut être comparée à un cours d’eau : lorsque le flux est suffisant, la stagnation microbienne est limitée ; en revanche, un ralentissement du courant favorise l’accumulation et la prolifération des micro-organismes.

Image tirée d’une conférence du Dr Siebecker 2021
Voyons maintenant plus en détail les maladies auto-immunes davantage touchées par le SIBO.
SIBO & hypothyroïdie
Des études ont reporté que le SIBO (prolifération de bactéries au niveau de l’intestin grêle) serait présent chez plus de 50% des personnes atteintes d’hypothyroïdie.
Une étude menée chez 50 personnes atteintes d’hypothyroïdie d’origine auto-immune (Hashimoto) a montré que 27 (54%) d’entre elles étaient positives au SIBO. À l’inverse, seules 2 personnes sur 40 (2%) du groupe contrôle ont été testées positives.
Les personnes positives au SIBO avaient des troubles digestifs (inconfort abdominal, flatulence, ballonnements) beaucoup plus marqués que les autres. Suite à un traitement antibiotique (rixafimin), les troubles digestifs des personnes ayant un SIBO ont diminué de manière significative.
Aussi, les études suggèrent que les personnes ayant des troubles digestifs et des signes d’hypothyroïdie devraient être testées pour vérifier l’hypothèse d’une prolifération microbienne dans l’intestin grêle (Lauritano et al., 2007; Patil, 2014).
Dans la même idée, en cas de SIBO associé à des signes d’hypothyroïdie qui persistent, un bilan thyroïdien correctement interprété est vivement conseillé.
En fonction des causes identifiées, un protocole de soutien des fonctions thyroïdiennes (mais pas que) sera proposé de façon individualisée.
SIBO & maladie cœliaque
Selon les études, 9% à 55% des patients ayant la maladie cœliaque ont été diagnostiqués d’un SIBO (Bures et al., 2010; Krauss & Schuppan, 2006; Rubio-Tapia et al., 2009). La prévalence semble s’élevée si la personne ne respecte pas une alimentation sans gluten stricte et/ou a également une intolérance au lactose (Ghoshal et al., 2004).
En cas de symptômes persistants même après l’arrêt stricte du gluten, le SIBO doit être une piste à explorer (Shah et al., 2022).
SIBO & MICI (Crohn & RCH)
Le SIBO est une complication réelle, mais malheureusement peu reconnue de la maladie de Crohn. D’ailleurs, le SIBO peut faire penser à une rechute de la maladie. Il est essentiel de creuser cette piste avec votre thérapeute si cette hypothèse semble plausible (Klaus et al., 2009).
SIBO est retrouvé dans 25% des patients atteints de la maladie de Crohn, et ce chiffre monte à 30% pour les personnes ayant eu une chirurgie (Castiglione et al., 2003). Cette forte prévalence est associée à la perte de la valve iléo fécale post chirurgie. Une fistule peut aussi être un facteur de risque.
Bien que contrairement à la maladie de Crohn, la rectocolite hémorragique affecte uniquement le colon/anus, le SIBO est aussi à considérer. Les études montrent que la présence de molécules pro- inflammatoires excessive associée et la diminution des antioxydants observée chez les patientes atteintes de RCH peut induire un stress oxydatif affectant la motilité du grêle, et donc induire un SIBO (Rana et al., 2014; Yang et al., 2021).
SIBO & sclérodermie systémique
On observe une atteinte du tube digestif chez près de 90 % des patients atteints de sclérodermie systémique (Morrisroe et al., 2020). Le SIBO serait présent chez environ 39 % de ces patients, et les deux tiers d’entre eux montrent une amélioration significative des symptômes après un traitement antibiotique.
Il est essentiel d’agir également sur la motilité intestinale pour prévenir les récidives ou, à défaut, en prolonger l’intervalle entre les épisodes.
SIBO & spondylarthrite ankylosante
Une étude a mis en évidence une prévalence plus forte au SIBO chez les participants atteints de spondylarthrite ankylosante sans que cette prévalence soit lié à l’activité de la maladie (Garcia et al., 2019). Aussi, il est intéressant de vérifier l’hypothèse d’un SIBO en présence de symptômes.
Conclusion
Le SIBO est une condition fréquente dans de nombreuses maladies auto-immunes.
Il est indispensable de le prendre en charge, car l’excès de bactéries peut entraîner des complications telles que des carences nutritionnelles, une hyperperméabilité intestinale et une inflammation persistante — autant de facteurs susceptibles d’entretenir ou d’aggraver le terrain auto-immun.
Cependant, l’éradication bactérienne seule, sans prise en compte des causes sous-jacentes du SIBO/IMO (troubles de la motricité digestive, hypochlorhydrie, adhérences, dysfonction immunitaire, etc.), expose à un risque élevé de récidive. Une approche globale visant à corriger les facteurs favorisants, restaurer l’écosystème intestinal et soutenir l’état nutritionnel est donc essentielle pour obtenir des résultats durables.
Le microbiote intestinal se comporte un peu comme une forêt : on peut éliminer les espèces envahissantes, mais si le sol, le climat et l’équilibre global ne sont pas restaurés, elles repousseront. En médecine fonctionnelle comme en écologie, la stabilité vient toujours du terrain.
La communauté BEAI : votre refuge biologique
Vous vivez avec une maladie auto-immune et vous vous sentez parfois isolé·e dans votre parcours ? Vous aimeriez échanger avec des personnes qui comprennent vraiment ce que vous vivez au quotidien ?
La Communauté BEAI est pensée comme un espace de co-régulation et de soutien mutuel.
Un lieu où :
✨ Vous pouvez partager vos victoires et vos difficultés sans jugement
✨ Vous trouvez des réponses à vos questions sur la gestion quotidienne de votre maladie
✨ Vous bénéficiez du soutien d'autres personnes qui vivent des défis similaires
✨ Vous bénéficiez d'appels mensuels pour des mini-consultations et des cercles de paroles
✨ Vous accédez à des ressources exclusives et des échanges avec des experts
Parce que comme nous venons de le voir, la qualité de vos connexions sociales influence directement votre inflammation, votre niveau de stress et votre capacité de récupération.
La Communauté BEAI privée n'est pas qu'un groupe Facebook. C'est un véritable écosystème de soutien conçu pour vous aider à construire ces liens nourriciers, prévisibles et soutenants dont votre corps a biologiquement besoin.
Références scientifiques
Bures, J., Cyrany, J., Kohoutova, D., Förstl, M., Rejchrt, S., Kvetina, J., Vorisek, V., & Kopacova, M. (2010). Small intestinal bacterial overgrowth syndrome. World journal of gastroenterology: WJG, 16(24), 2978.
Castiglione, F., Rispo, A., Di Girolamo, E., Cozzolino, A., Manguso, F., Grassia, R., & Mazzacca, G. (2003). Antibiotic treatment of small bowel bacterial overgrowth in patients with Crohn's disease. Alimentary pharmacology & therapeutics, 18(11-12), 1107-1112.
Frasier, K., Farber, M., Daly, P., Vinagolu-Baur, J., & Hassan, M. (2025). Epidermal Manifestations of Small Intestinal Bacterial Overgrowth and the Connection to Microbial Inflammation. Ameri J Clin Med Re: AJCMR-220.
Garcia, O. E. O., Cerpa-Cruz, S., Gutierrez-Ureña, S., Martinez-Bonilla, G., Medina, A. G. B., Gonzalez- Diaz, V., Velazco, J. A. V. R., & Cruz, L. I. H. (2019). THU0396 SMALL INTESTINAL BACTERIA OVERGROWTH IN SPONDYLOARTHRITIS. In: BMJ Publishing Group Ltd.
Ghoshal, U. C., Ghoshal, U., Misra, A., & Choudhuri, G. (2004). Partially responsive celiac disease resulting from small intestinal bacterial overgrowth and lactose intolerance. BMC gastroenterology, 4(1), 1-6.
Klaus, J., Spaniol, U., Adler, G., Mason, R. A., Reinshagen, M., & von Tirpitz C, C. (2009). Small intestinal bacterial overgrowth mimicking acute flare as a pitfall in patients with Crohn's Disease. BMC gastroenterology, 9, 1-8.
Krauss, N., & Schuppan, D. (2006). Monitoring nonresponsive patients who have celiac disease. Gastrointestinal endoscopy clinics of North America, 16(2), 317-327.
Lauritano, E. C., Gabrielli, M., Scarpellini, E., Lupascu, A., Novi, M., Sottili, S., Vitale, G., Cesario, V., Serricchio, M., & Cammarota, G. (2008). Small intestinal bacterial overgrowth recurrence after antibiotic therapy. Official journal of the American College of Gastroenterology| ACG, 103(8), 2031-2035.
Pimentel, M., Saad, R. J., Long, M. D., & Rao, S. S. (2020). ACG clinical guideline: small intestinal bacterial overgrowth. Official journal of the American College of Gastroenterology| ACG, 115(2), 165-178.
Rana, S. V., Sharma, S., Kaur, J., Prasad, K. K., Sinha, S. K., Kochhar, R., Malik, A., & Morya, R. K. (2014). Relationship of cytokines, oxidative stress and GI motility with bacterial overgrowth in ulcerative colitis patients. Journal of Crohn's and Colitis, 8(8), 859-865.
Rubio-Tapia, A., Barton, S. H., Rosenblatt, J. E., & Murray, J. A. (2009). Prevalence of small intestine bacterial overgrowth diagnosed by quantitative culture of intestinal aspirate in celiac disease. Journal of clinical gastroenterology, 43(2), 157.
Shah, A., Thite, P., Hansen, T., Kendall, B. J., Sanders, D. S., Morrison, M., Jones, M. P., & Holtmann, G. (2022). Links between celiac disease and small intestinal bacterial overgrowth: A systematic review and meta-analysis. Journal of Gastroenterology and Hepatology, 37(10), 1844-1852.
Shang, L., Zhang, T., Liu, X., Wang, H., Gao, C., Zhao, J., Xiao-Feng, L., & Gao, H. (2019). AB0034 increased production of hydrogen and methane suggested bacterial overgrowth in the small intestine in patients with autoimmune disease detected by lactulose breath tests. Annals of the rheumatic diseases, 78, 1482-1483.
Yang, C., Zhang, X., Wang, S., Huo, X., & Wang, J. (2021). Small intestinal bacterial overgrowth and evaluation of intestinal barrier function in patients with ulcerative colitis. American Journal of Translational Research, 13(6), 6605.
Article rédigé par : Juliette Janvresse, Dietéticienne & Coach AIP
Bien-être Auto-immune
L'expert des maladies auto-immunes
"Ensemble, vers la santé auto-immune !"





Commentaires